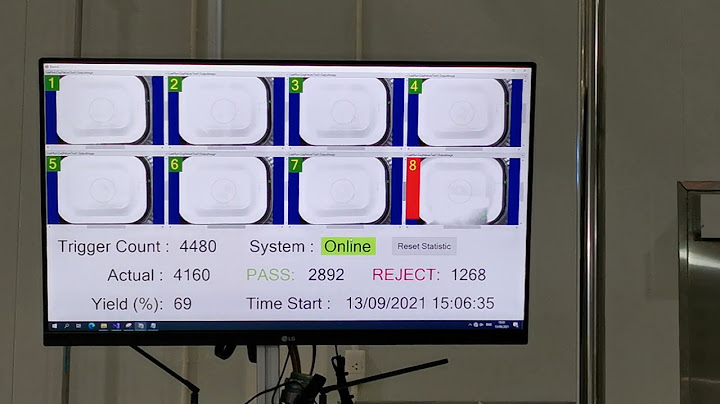
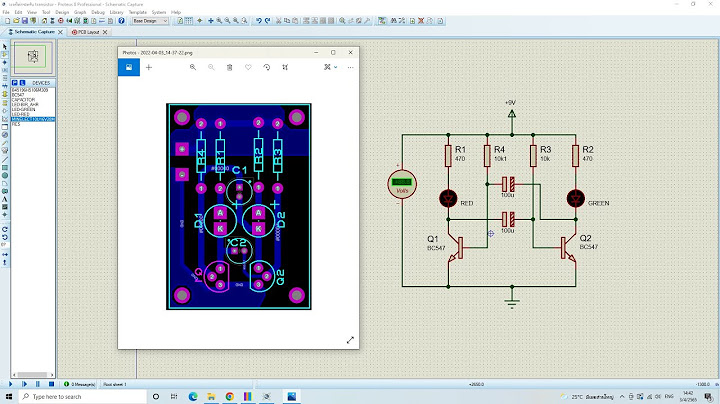
จากวิกิพีเดีย สารานุกรมเสรี เลขมวล (mass number, A), หรือ เลขมวลอะตอม หรือ เลขนิวคลีออน เป็นผลรวมของจำนวนโปรตอนและนิวตรอน (โปรตอนและนิวตรอนเรียกรวมกันว่านิวคลีออน) ในนิวเคลียสอะตอม เพราะโปรตอนและนิวตรอนต่างก็เป็นแบริออน เลขมวล A ก็คือเลขแบริออน B ของนิวเคลียสของอะตอมหรือไอออน เลขมวลจะต่างกันถ้าเป็นไอโซโทปที่ต่างกันของธาตุเคมี เลขมวลไม่เหมือนกับเลขอะตอม (Z) ที่แสดงถึงจำนวนโปรตอนในนิวเคลียสและสามารถใช้ระบุบธาตุได้ ดังนั้นค่าที่ต่างกันระหว่างเลขมวลและเลขอะตอมจะบ่งบอกถึงจำนวนนิวตรอน (N) ในนิวเคลียส: N=A−Z[1] เลขมวลจะถูกเขียนอยู่ด้านหลังหรือมุมบนด้านซ้ายของสัญลักษณ์ธาตุ เช่น ไอโซปโทปปกติของคาร์บอนคือ คาร์บอน-12 หรือ 12C ซึ่งมี 6 โปรตรอนและ 6 นิวตรอน สัญลักษณ์ไอโซปแบบเต็มรูปแบบจะมีเลขอะตอม (Z) ด้วยอยู่ด้านล่างซ้ายมือของสัญลักษณ์ธาตุ: 6C[2] ซึ่งวิธีนี้ไม่มีความจำเป็นนักจึงนิยมละเลขอะตอมไว้ ตัวอย่าง: การสลายในธรรมชาติของคาร์บอน-14จะแผ่รังสีเบต้า ด้วยวิธีนิวตรอนหนึ่งตัวถูกทำให้เปลี่ยนสถานะกลายเป็นโปรตอนกับการปล่อยพลังงานของอิเล็กตรอนและอนุภาคต้าน ดังนั้นเลขอะตอมจะเพิ่มขึ้น 1 (Z: 6→7) และเลขมวลมีค่าเท่าเดิม (A = 14) ขณะที่เลขนิวตรอนลดลง 1 (n: 8→7) [3] อะตอมผลลัพธ์เป็นอะตอมไนโตรเจน-14ซึ่งมี 7 โปรตอนและ 7 นิวตรอน: 6C → 7N + e- + veยูเรเนียม-238ปกติจะสลายให้รังสีแอลฟาซึ่งนิวเคลียสเสีย 2 นิวตรอนและ 2 โปรตรอนในรูปแบบของอนุภาคแอลฟา ดังนั้นเลขอะตอมและเลขนิวตรอนจะลดลงไป 2 (Z: 92→90, n: 146→144) ซึ่งเลขมวลจะลดไป 4 (A = 238→234) อะตอมผลลัพธ์เป็นอะตอมทอเรียม-234 และอนุภาคแอลฟา (2He2+) :[4] อ้างอิง[แก้]
_______จากการศึกษาเกี่ยวกับโครงสร้างของอะตอม โดยมีข้อมูลต่างๆ จากการทดลองมาสนับสนุน สรุปได้ว่า อะตอมของธาตุต่างๆ จะประกอบด้วยอิเล็กตรอน โปรตอนและนิวตรอน (ยกเว้นอะตอมของธาตุไฮโดรเจน ที่ไม่มีนิวตรอน) ซึ่งมีจำนวนแตกต่างกันไป เลขที่แสดงจ้านวนโปรตอนในนิวเคลียสของอะตอม เรียกว่าเลขอะตอม (atomic number, Z) เลขอะตอมจะเป็นค่าเฉพาะของธาตุ ธาตุชนิดเดียวกันจะมีเลขอะตอมเท่ากันเสมอ ซึ่งที่สภาวะปกติจะมีจำนวนโปรตอนและอิเล็กตรอนเท่ากัน ส่วนเลขที่แสดงจำนวนผลบวกของโปรตอนและจำนวนนิวตรอน เราเรียกว่า เลขมวล (mass number, A) ซึ่งในนิวเคลียสของอะตอม เลขมวลจะมีค่าใกล้เคียงกับเลขของอะตอม โดยผลต่างของเลขมวลกับเลขของอะตอมจะเท่ากับจำนวนนิวตรอนโดยสามารถเขียนสัญลักษณ์นิวเคลียร์ได้ คือ ที่มา : http://wasita2536338.blogspot.com/p/24-28-2554.html เลขอะตอม คือ จำนวนโปรตอนในนิวเคลียสของแต่ละอะตอมของธาตุ ในอะตอมที่เป็นกลางจะมีจำนวนโปรตอนเท่ากับจ้านวนอิเล็กตรอน ดังนั้นเลขเชิงอะตอมจึงบอกจำนวนของอิเล็กตรอนของธาตุได้ด้วย เนื่องจากอะตอมของธาตุชนิดเดียวกันมีค่าเลขเชิงอะตอมเท่ากันเสมอ เลขเชิงอะตอมจึงป็นเอกลักษณ์ของธาตุชนิดเดียวกัน เช่น เลขเชิงอะตอมของฟอสฟอรัสเท่ากับ 15 นั้นคือทุกๆ อะตอมที่เป็นกลางของฟอสฟอรัสจะมี 15 โปรตอน และมี 15 อิเล็กตรอน และกล่าวได้ว่าอะตอมใดๆ ในจักรวาลถ้ามี 15 โปรตอนแล้ว จะเรียกว่า “ฟอสฟอรัส” ทั้งสิ้น
เลขมวล คือ ผลรวมของนิวตรอนและโปรตอนที่มีในนิวเคลียสของอะตอมของธาตุ นิวเคลียสในอะตอมอื่นๆ |

กระทู้ที่เกี่ยวข้อง
การโฆษณา
ข่าวล่าสุด
การโฆษณา
ผู้มีอำนาจ
การโฆษณา
ถูกกฎหมาย
ช่วย

ลิขสิทธิ์ © 2024 th.ketajaman Inc.